“氢锂钠钾铷铯钫”、“铍镁钙锶钡镭”,大陆和台湾学生一定经历过,化学课埋头苦背元素周期表,相信即使告别学生时代,许多民众多少还能背上个几句。最近日本论坛上,有位网友转贴了中文版元素周期表,意外引起日本人热烈讨论。
日本多数网友看到中文版元素周期表相当震惊,佩服这么多复杂笔画写成,又无比相像的中文字,还要能一一背起来。有人说像“将棋”、有人说像“麻将”,还有人说完全是“咒语”,当然也有网友相当感恩,“好在我生在日本”。
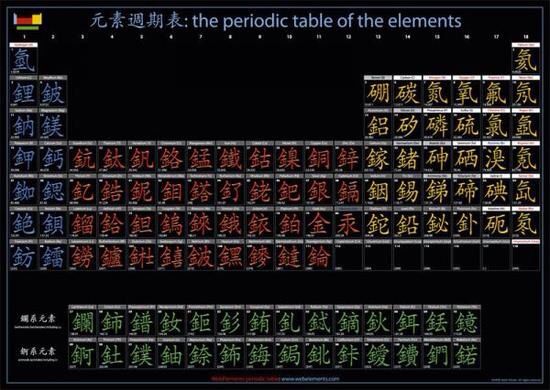
元素周期表
氢锂钠钾铷铯钫——请李娜加入私访
铍镁钙锶钡镭——媲美盖茨被雷
硼铝镓铟铊——碰女嫁音他
碳硅锗锡铅——探归者西迁
氮磷砷锑铋——蛋临身体闭
氧硫硒碲钋——养牛西蹄扑
氟氯溴碘砹——父女绣点爱
氦氖氩氪氙氡——害耐亚克先动
一、
元素周期表中元素及其化合物的递变性规律
1、原子半径
(1)除第1周期外,其他周期元素(惰性气体元素除外)的原子半径随原子序数的递增而
减小;
(2)同一族的元素从上到下,随电子层数增多,原子半径增大。
2、元素化合价
(1)除第1周期外,同周期从左到右,元素最高正价由碱金属
+1递增到+7
,非金属元素负价由碳族-4
递增到-1
(氟无正价,氧无+6价,除外);
(2)同一主族的元素的最高正价、负价均相同。
3、单质的熔点
(1)同一周期元素随原子序数的递增,元素组成的金属单质的熔点递增,非金属单质的熔
点递减;
(2)同一族元素从上到下,元素组成的金属单质的熔点递减,非金属单质的熔点递增。
4、元素的金属性与非金属性
(1)同一周期的元素从左到右金属性递减,非金属性递增;
(2)同一主族元素从上到下金属性递增,非金属性递减。
5、最高价氧化物和水化物的酸碱性
元素的金属性越强,其最高价氧化物的水化物的碱性越强;元素的非金属性越强,最高价
氧化物的水化物的酸性越强。
6、非金属气态氢化物
元素非金属性越强,气态氢化物越稳定。同周期非金属元素的非金属性越强,其气态氢化
物水溶液一般酸性越强;
同主族非金属元素的非金属性越强,
其气态氢化物水溶液的酸性越弱。
7、单质的氧化性、还原性
一般元素的金属性越强,其单质的还原性越强,其氧化物的氧离子氧化性越弱;元素的非
金属性越强,其单质的氧化性越强,其简单阴离子的还原性越弱。
二、推断元素位置的规律
判断元素在周期表中位置应牢记的规律:
1、元素周期数等于核外电子层数;
2、主族元素的序数等于最外层电子数;
3、确定族数应先确定是主族还是副族,
其方法是采用原子序数逐步减去各周期的元素种数,
即可由最后的差数来确定。最后的差数就是族序数,差为
最后的差数就是族序数,差为8、9、10时为VIII族,差数大于10时,则再减去10,最后结果为族序数。